Tratamiento con crioablación para cáncer de próstata
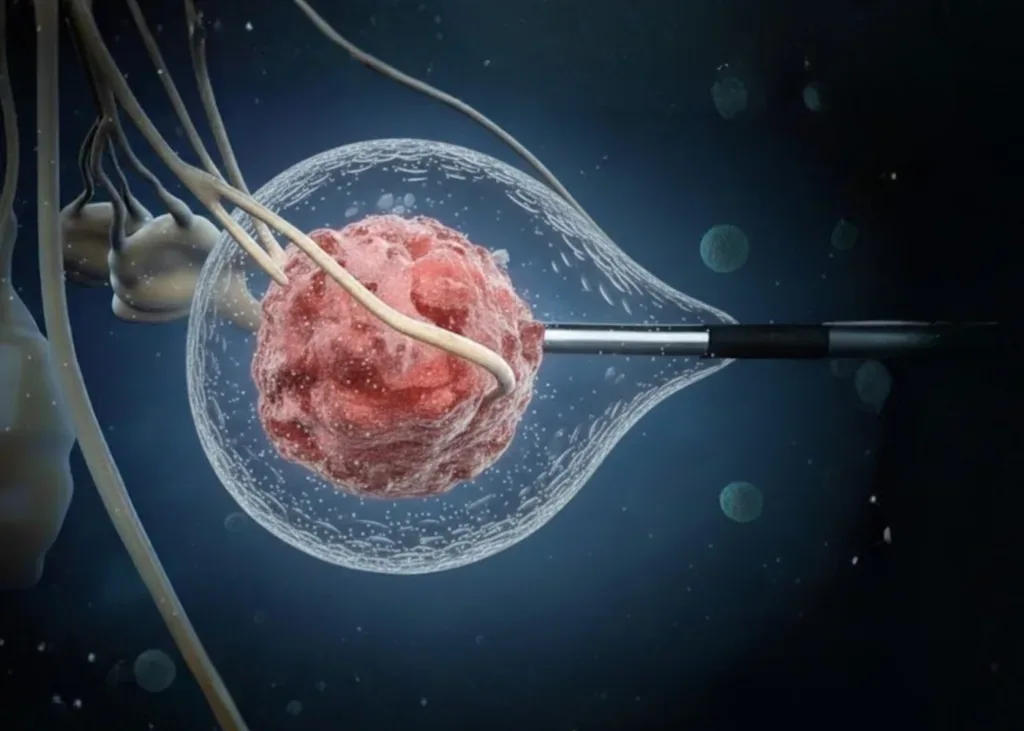
Tratamiento con crioablación para cáncer de próstata: Procedimiento y resultados La crioablación de próstata se ha consolidado en 2026 como una de las herramientas más potentes y precisas de la urología moderna. A diferencia de la cirugía tradicional, este tratamiento no utiliza bisturíes para remover tejidos; en su lugar, emplea el poder del frío extremo para aniquilar las células cancerosas desde el interior, protegiendo la integridad del paciente. Este procedimiento de mínima invasión ofrece una alternativa definitiva para quienes buscan eliminar el tumor con una recuperación acelerada y efectos secundarios mínimos. En este artículo, desglosaremos paso a paso cómo funciona la tecnología de crioablación para el cáncer de próstata, qué esperar durante la intervención y cuáles son los resultados clínicos que respaldan su eficacia en el control del cáncer de próstata. ¿Qué es la crioablación de próstata y cómo destruye el cáncer? La crioablación, también llamada criocirugía, es una técnica de ablación térmica que utiliza temperaturas bajo cero para causar la muerte celular programada del tejido maligno. Es un proceso físico controlado donde el frío se convierte en el agente terapéutico, permitiendo una destrucción celular completa sin necesidad de incisiones abdominales. El uso de gas argón para la congelación celular extrema. La base tecnológica de este tratamiento es el uso de gas argón de alta pureza. A través de aplicadores ultrafinos conocidos como criosondas, el gas se expande rápidamente, generando un descenso de temperatura que alcanza los -40°C en segundos. Este enfriamiento extremo congela el agua dentro y fuera de las células cancerosas, formando cristales de hielo que rompen las membranas celulares. Al interrumpir el suministro de sangre al tumor y destruir su estructura interna, el cáncer es eliminado de manera efectiva y segura. ¿Cómo se forma la «bola de hielo» que aniquila el tumor? El éxito de la crioablación para el cáncer de prostata reside en la formación de una «bola de hielo» controlada. El especialista monitorea en tiempo real, mediante ultrasonido de alta resolución, cómo se expande esta esfera de congelación alrededor del tumor. Gracias a este control visual constante, el médico puede ajustar la intensidad del frío para asegurar que la bola de hielo cubra la totalidad de la lesión maligna (margen de seguridad), mientras utiliza sensores térmicos para proteger los tejidos sanos circundantes, como el recto y el esfínter urinario. Es un proceso donde el objetivo es la precisión absoluta. ¿Cómo es el procedimiento de crioablación paso a paso? La crioablación se realiza en un entorno quirúrgico especializado, pero bajo un enfoque de mínima invasión. A diferencia de una cirugía abierta que puede durar varias horas, este procedimiento suele completarse en un lapso de 60 a 90 minutos, dependiendo de la extensión del área a tratar. Preparación del paciente y uso de anestesia. El proceso comienza con la preparación estándar para asegurar la comodidad total del paciente. Generalmente, se utiliza anestesia regional (epidural) o general leve, lo que garantiza que no exista ningún tipo de dolor durante la intervención. Una vez anestesiado, el paciente se coloca en una posición que permite al urólogo acceder a la próstata con la mayor precisión posible a través del área del periné (el espacio entre el escroto y el ano), evitando cualquier incisión abdominal. Guía por ultrasonido en tiempo real para una precisión milimétrica. La clave de la crioablación es la visibilidad total. El médico utiliza una sonda de ultrasonido transrectal de alta resolución que proyecta una imagen en vivo de la próstata en monitores quirúrgicos. Colocación de criosondas: Bajo esta guía visual, se introducen agujas ultrafinas (criosondas) directamente en el tumor. Gracias a la imagen digital, el médico puede ver exactamente dónde se posiciona cada aguja. Monitoreo térmico: Se colocan sensores de temperatura cerca del recto y la uretra. Estos sensores actúan como un sistema de seguridad que alerta al médico si el frío se acerca demasiado a tejidos sanos. Ciclos de congelación: Se activan los flujos de gas argón para crear la «bola de hielo». Normalmente se realizan dos ciclos de congelación y descongelación para asegurar la destrucción completa de las células malignas. Calentamiento uretral: Durante todo el proceso, se utiliza un catéter de calentamiento especial para proteger la uretra, asegurando que el flujo urinario no se vea afectado por las bajas temperaturas. Al finalizar, se retiran las criosondas y, al no haber cortes que suturar, solo se coloca un pequeño vendaje en el área de entrada. ¿Qué resultados se esperan tras una crioablación de próstata? Al evaluar un tratamiento contra el cáncer, la efectividad se mide en dos dimensiones: el control de la enfermedad y la preservación de la calidad de vida. En 2026, la crioablación como tratamiento para el cáncer de próstata ha demostrado ser una herramienta de alta eficacia oncológica, permitiendo que el paciente recupere su salud sin heredar las secuelas físicas que antes se consideraban «el costo inevitable» de curarse. Tasas de éxito en el control oncológico a largo plazo. Los estudios clínicos más recientes confirman que la crioablación ofrece tasas de control del cáncer comparables a la cirugía radical en pacientes bien seleccionados (aquellos con tumores localizados de riesgo bajo o intermedio). Eliminación del tumor: Al congelar el tejido a -40°C, se garantiza la destrucción celular inmediata. Seguimiento con PSA: Tras el procedimiento, los niveles de Antígeno Prostático (PSA) suelen descender drásticamente y mantenerse estables, lo que indica que el foco de células malignas ha sido erradicado con éxito. Opción de repetición: A diferencia de la radioterapia, si en el futuro apareciera una nueva lesión en otra zona de la próstata, la crioablación puede volver a realizarse, ofreciendo una flexibilidad terapéutica única. ¿Cómo impacta este tratamiento en la función eréctil y urinaria? Este es el punto donde la crioablación supera a los métodos tradicionales. Al ser un tratamiento focalizado, el impacto en la vida íntima y social del hombre es mínimo: Control urinario (Continencia): Gracias al uso de catéteres de calentamiento que protegen la uretra durante la congelación, el riesgo de incontinencia urinaria es inferior al 1% en la mayoría de las
Terapia focal en cáncer de próstata: ¿Qué es y quién es candidato?
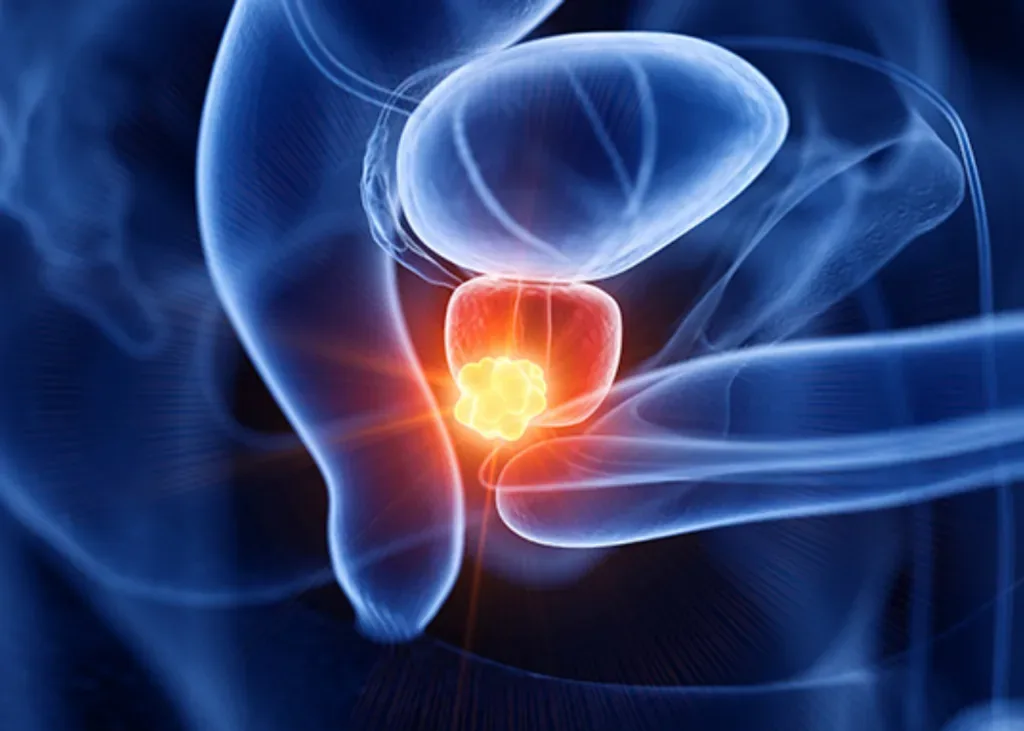
Terapia focal en cáncer de próstata: ¿Qué es y quién es candidato? El avance de la tecnología médica ha permitido que el tratamiento del cáncer de próstata deje de ser una intervención «todo o nada». Hoy en día, la terapia focal se posiciona como la alternativa de precisión para aquellos hombres que buscan eliminar el tumor sin los efectos secundarios drásticos de la cirugía radical. A diferencia de los métodos tradicionales, la terapia focal no remueve la glándula completa; se enfoca exclusivamente en destruir el tejido maligno mediante energías dirigidas. Este enfoque de mínima invasión permite que el paciente conserve su calidad de vida, protegiendo funciones vitales como la potencia sexual y el control urinario. En este artículo, exploraremos qué es exactamente esta tecnología y cuáles son los criterios clínicos para saber si eres el candidato ideal para este procedimiento de vanguardia. ¿Qué es la terapia focal y cómo se diferencia de la cirugía radical? Para entender el valor de la terapia focal, debemos compararla con el estándar histórico: la cirugía radical (prostatectomía). Mientras que la cirugía extrae toda la próstata para asegurar que no quede rastro de enfermedad, la terapia focal utiliza un concepto de «Tratamiento de Precisión». El concepto de «Tratamiento de Precisión»: atacar el tumor, no el órgano. La terapia focal trata a la próstata de la misma manera que un dermatólogo trata una lesión en la piel: se elimina solo la zona afectada. Utilizando guías de imagen avanzada, el especialista identifica la ubicación exacta del tumor y aplica energía (frío o pulsos eléctricos) para destruirlo in situ. Al dejar intacto el resto de la glándula sana, el impacto en el cuerpo es significativamente menor. ¿Por qué la terapia focal reduce los efectos secundarios? La razón principal es la preservación de estructuras anatómicas críticas. Alrededor de la próstata se encuentran los haces de nervios cavernosos (responsables de la erección) y el esfínter urinario. En una cirugía radical, estas estructuras están en alto riesgo de manipulación o daño. En cambio, la terapia focal permite mantener una distancia de seguridad, reduciendo drásticamente las probabilidades de impotencia o incontinencia urinaria, lo que permite al paciente una recuperación funcional casi inmediata. ¿Cuáles son los requisitos para ser candidato a terapia focal? No todos los diagnósticos de cáncer de próstata requieren una cirugía radical, pero tampoco todos son aptos para la terapia focal. La clave del éxito de este tratamiento reside en una selección rigurosa del paciente. El candidato ideal es aquel cuyo tumor es detectable, está localizado y presenta un comportamiento biológico que permite una intervención dirigida de mínima invasión. Cáncer de próstata de bajo riesgo y tumores localizados. El requisito fundamental es que el cáncer se encuentre en una etapa localizada, es decir, que las células malignas estén confinadas estrictamente dentro de la glándula prostática. Si el cáncer ha comenzado a extenderse a los ganglios linfáticos o a los huesos (metástasis), la terapia focal deja de ser la opción primaria, ya que se requiere un enfoque sistémico. Además, se busca que el tumor sea «unifocal» o que tenga un foco dominante claro. Gracias a la tecnología de imagen actual, podemos identificar con precisión esa «zona caliente» para tratarla sin afectar el resto del órgano. ¿Qué papel juega el puntaje de Gleason y el nivel de PSA? Para determinar la elegancia de este tratamiento, los médicos nos basamos en dos indicadores críticos que aparecen en tus resultados de laboratorio: Puntaje de Gleason: Este valor mide qué tan agresivas se ven las células bajo el microscopio. Los candidatos ideales suelen tener un Gleason de 6 o 7 (3+4). Un puntaje mayor indica una agresividad que podría requerir tratamientos más extensos. Nivel de Antígeno Prostático (PSA): Generalmente, se busca que el PSA sea menor a 10-15 ng/ml. Un nivel de PSA muy elevado podría ser señal de que el cáncer es más extenso de lo que muestran las imágenes iniciales. ¿Qué estudios se necesitan para calificar a este tratamiento? Para que un médico determine si eres candidato a una terapia focal de mínima invasión, la evaluación debe ir más allá del tacto rectal o un análisis de sangre básico. Necesitamos «ver» el tumor con una claridad milimétrica. En 2026, el estándar de oro para esta calificación combina la imagenología avanzada con la patología dirigida. La importancia de la Resonancia Magnética Multiparamétrica (mpMRI). La resonancia magnética multiparamétrica es el pilar del diagnóstico moderno. A diferencia de un ultrasonido convencional, este estudio permite observar la próstata en diferentes «planos» y secuencias, identificando áreas sospechosas que antes eran invisibles. Este estudio nos proporciona una calificación llamada PI-RADS. Si tu resultado muestra una zona PI-RADS 4 o 5, significa que hay un área con alta probabilidad de ser un tumor significativo que puede ser atacado directamente con terapia focal, protegiendo el resto de la glándula que se observa sana. Biopsia por fusión: el mapa exacto para localizar el cáncer. Una vez identificado el punto sospechoso en la resonancia, el siguiente paso es la biopsia por fusión de imágenes. Este es un procedimiento tecnológico donde superponemos las imágenes de la resonancia magnética sobre un ultrasonido en tiempo real. Precisión quirúrgica: En lugar de tomar muestras al azar (como en la biopsia tradicional), el médico dirige la aguja exactamente al centro de la lesión detectada. Confirmación de idoneidad: Este estudio confirma si el cáncer es unifocal (está en un solo sitio) y nos da el puntaje de Gleason exacto de esa zona. Sin este «mapa de navegación», no sería posible garantizar que las terapias focales de mínima invasión eliminen el tejido correcto. Es la diferencia entre disparar a ciegas y utilizar un sistema de guía láser. Tipos de terapia focal: Crioablación y Electroporación (IRE) En la medicina de precisión actual, contamos con dos herramientas principales para realizar una terapia focal efectiva. Ambas comparten el objetivo de ser de mínima invasión, pero utilizan mecanismos físicos distintos para eliminar el cáncer. La elección entre una u otra dependerá de un análisis detallado de la anatomía de tu próstata y la
¿Cuáles son los nuevos tratamientos para el cáncer de próstata?

¿Cuáles son los nuevos tratamientos para el cáncer de próstata? Un diagnóstico de cáncer de próstata ya no tiene por qué comprometer tu estilo de vida. Aunque los métodos tradicionales suelen dejar secuelas físicas y emocionales, la urología moderna ha evolucionado hacia nuevos tratamientos para el cáncer de próstata buscando la precisión digital y la mínima invasión. Hoy, el objetivo es erradicar las células malignas preservando la integridad del cuerpo. Gracias a los nuevos tratamientos, los pacientes acceden a alternativas con recuperación récord que mantienen intactas funciones vitales como la continencia y la potencia sexual. En este artículo, exploramos cómo las tecnologías avanzadas transforman el diagnóstico en una oportunidad para sanar sin sacrificar tu bienestar. ¿Qué opciones de tratamiento tradicional existen para el cáncer de próstata? Para valorar el alcance de las nuevas tecnologías, es necesario entender el punto de partida: los tratamientos que han sido el estándar durante décadas. Aunque han salvado millones de vidas, su enfoque suele ser «radical», lo que significa que tratan a la próstata como un todo, a menudo afectando los tejidos sanos que la rodean. La prostatectomía radical y el enfoque de la cirugía abierta. La prostatectomía radical consiste en la remoción quirúrgica completa de la glándula prostática y algunos tejidos circundantes. Durante mucho tiempo, la cirugía abierta fue la única vía para asegurar la eliminación del cáncer. En este procedimiento, el cirujano realiza una incisión extensa para extraer la glándula manualmente. Si bien es una técnica probada para el control oncológico, su naturaleza invasiva conlleva riesgos inherentes. Al ser una zona densamente poblada por nervios delicados y esfínteres, la manipulación quirúrgica puede derivar en complicaciones que alteran la cotidianidad del paciente, además de requerir periodos de hospitalización y recuperación prolongados. Radioterapia como tratamiento del cáncer de próstata La radioterapia es la otra columna vertebral del tratamiento tradicional. Utiliza altas dosis de radiación para destruir las células cancerosas o impedir que crezcan. Aunque evita el quirófano, la radiación no siempre es selectiva. El principal desafío de la radioterapia convencional es el daño colateral a los órganos vecinos, como la vejiga y el recto. Esto puede manifestarse en síntomas crónicos como urgencia urinaria, sangrado o inflamación intestinal. Además, los efectos sobre la función eréctil pueden no aparecer de inmediato, sino desarrollarse meses o años después de concluir las sesiones, lo que genera una incertidumbre constante en el paciente sobre su salud a largo plazo. ¿Qué es la vigilancia activa y cuándo es una opción segura? La vigilancia activa es una estrategia médica diseñada para hombres con un cáncer de próstata de bajo riesgo o crecimiento muy lento. En lugar de proceder de inmediato con una cirugía o radioterapia, el equipo médico monitorea el tumor de manera estricta y periódica. El objetivo es evitar el sobretratamiento y los efectos secundarios innecesarios, interviniendo únicamente si el cáncer muestra señales de volverse más agresivo. Casos específicos donde se puede evitar la prostatectomía. No todos los pacientes son candidatos para este enfoque. La vigilancia activa se considera una opción segura y preferible bajo criterios clínicos muy específicos: Puntaje de Gleason bajo: Cuando las células cancerosas se ven muy similares a las sanas bajo el microscopio (generalmente un Gleason de 6). Niveles estables de Antígeno Prostático (PSA): Si los análisis de sangre muestran que los niveles de PSA se mantienen bajos y no suben rápidamente. Tumores localizados y pequeños: Cuando el cáncer está confinado a una pequeña área de la próstata y no hay evidencia de que se esté extendiendo. Este método no significa «no hacer nada». Implica un compromiso del paciente para realizarse biopsias, resonancias magnéticas y pruebas de PSA de forma regular, garantizando que siempre estemos un paso adelante de la enfermedad. ¿Qué son las terapias focales y cómo protegen la próstata? Si la vigilancia activa ya no es suficiente, pero una cirugía radical parece excesiva, entran en juego las terapias focales. Este es el punto medio revolucionario de la urología moderna. A diferencia de la cirugía tradicional que extrae toda la glándula, la terapia focal utiliza energía dirigida para destruir únicamente la zona donde se encuentra el tumor, dejando intacto el resto del tejido sano de la próstata. Es un enfoque similar a cómo se trata un tumor en la piel: se elimina la lesión, no el brazo completo. Al proteger las estructuras circundantes, como los haces de nervios y el esfínter urinario, estas terapias minimizan drásticamente el riesgo de impotencia y de incontinencia. Es la opción ideal para quienes buscan un control oncológico efectivo sin sacrificar su vida sexual ni su comodidad diaria. ¿En qué consisten los tratamientos de ablación prostática? La ablación prostática representa uno de los saltos más significativos en la urología del siglo XXI. En términos simples, «ablación» significa la destrucción de tejido mediante la aplicación directa de energía. A diferencia de la cirugía, donde se extrae la glándula completa para eliminar el problema, la ablación se enfoca en aniquilar las células cancerosas in situ (en su lugar), sin necesidad de remover la próstata. Este enfoque permite una precisión milimétrica: el médico puede dirigir la energía exactamente al núcleo del tumor, protegiendo los tejidos sanos que lo rodean. Es la base de lo que conocemos como «cirugía sin bisturí». Destrucción de células cancerosas sin necesidad de incisiones. Una de las mayores ventajas de la ablación es que es un procedimiento de mínima invasión. En lugar de grandes cortes abdominales, el tratamiento se realiza a través de aplicadores o agujas ultrafinas que se introducen con guía de imagen de alta resolución (como el ultrasonido o la resonancia magnética). Al no haber incisiones quirúrgicas tradicionales: El sangrado es mínimo o inexistente: Lo que reduce drásticamente las complicaciones postoperatorias. No hay cicatrices externas: El cuerpo no tiene que recuperarse de un trauma muscular o cutáneo mayor. Hospitalización ambulatoria: La mayoría de estos procedimientos permiten que el paciente regrese a su casa el mismo día o en menos de 24 horas. ¿Qué tan efectiva es la terapia de ablación para eliminar tumores? La efectividad de la
Factores de riesgo del cáncer de próstata: ¿Qué aumenta las probabilidades?

Factores de riesgo del cáncer de próstata: ¿Qué aumenta las probabilidades? En el ámbito de la oncología moderna, el éxito del tratamiento no comienza en el quirófano, sino mucho antes: en la identificación precisa de quién tiene mayores probabilidades de desarrollar la enfermedad. Los factores de riesgo del cáncer de próstata no son causas directas, sino variables biológicas y ambientales que, al combinarse, pueden alterar el comportamiento de las células prostáticas. Entender tu perfil de riesgo es fundamental para pasar de una medicina general a una urología de precisión. No todos los hombres requieren el mismo nivel de vigilancia; mientras que para algunos el monitoreo puede ser anual, para otros —con una carga genética o metabólica específica— la detección debe ser mucho más estrecha y apoyada en tecnologías de vanguardia. A continuación, analizaremos cómo la edad, la herencia y el estilo de vida interactúan para definir tu probabilidad estadística, permitiéndote tomar decisiones informadas sobre cuándo y cómo iniciar tu protocolo de diagnóstico preventivo. ¿A qué edad es más común el cáncer de próstata? El factor del envejecimiento celular. El factor de riesgo de desarrollar una neoplasia en la próstata es directamente proporcional a la edad. Estadísticamente, el cáncer de próstata es una enfermedad de la madurez; sin embargo, el enfoque médico actual no solo se centra en cuántos años tiene el paciente, sino en la calidad del envejecimiento celular de su glándula. El umbral de los 50 años y el tamizaje preventivo. La frontera de los 50 años marca el inicio del protocolo de vigilancia activa para la población general. A partir de esta década, la incidencia aumenta de forma exponencial. La razón clínica es que, tras décadas de exposición a hormonas (testosterona) y procesos metabólicos, la próstata alcanza un punto crítico donde la supervisión mediante el Antígeno Prostático Específico (PSA) se vuelve obligatoria para detectar cualquier anomalía antes de que sea palpable o sintomática. ¿Por qué las células prostáticas mutan con el tiempo? A nivel molecular, el envejecimiento implica una pérdida de eficiencia en los mecanismos de reparación del ADN. Cada vez que una célula prostática se divide, existe una pequeña probabilidad de que ocurra un error genético. En la juventud, el cuerpo identifica y elimina estas células defectuosas. Con el paso de los años, estas «instrucciones erróneas» se acumulan, permitiendo que células con capacidad de crecimiento descontrolado sobrevivan y formen tumores. Es lo que en urología conocemos como la acumulación de daño genómico. Casos prematuros: Riesgos antes de los 45 años. Aunque es poco frecuente, el diagnóstico en hombres menores de 45 años suele representar un desafío clínico mayor. Cuando el cáncer aparece de forma prematura, generalmente no se debe al desgaste natural por edad, sino a una predisposición genética agresiva. Estos tumores suelen tener una cinética de crecimiento más rápida, lo que subraya la importancia de conocer los antecedentes familiares para iniciar revisiones incluso antes de los 40 años si es necesario. Ubicación del problema: La zona de transición vs. la zona periférica Una de las mayores diferencias entre cáncer de próstata e hiperplasia radica en el lugar exacto donde se originan dentro de la glándula: Zona de Transición (HBP): La hiperplasia ocurre generalmente en la parte central de la próstata, la zona que rodea la uretra (el conducto por donde sale la orina). Al crecer hacia adentro, comprime la uretra rápidamente, lo que explica por qué la HBP suele dar síntomas urinarios muy pronto. Zona Periférica (Cáncer): La mayoría de los tumores malignos se originan en la periferia, es decir, en la parte externa de la próstata. Al estar lejos de la uretra, el cáncer puede crecer durante años sin obstruir el paso de la orina, lo que lo convierte en una enfermedad silenciosa que solo se detecta mediante estudios preventivos. ¿Es el cáncer de próstata hereditario? El peso de los antecedentes familiares. Cuando analizamos los factores de riesgo del cáncer de próstata, la carga genética ocupa un lugar central. No se trata simplemente de una coincidencia familiar; existen mecanismos biológicos heredados que pueden predeterminar la susceptibilidad de un hombre ante esta patología. Parientes de primer grado: Cuando el riesgo se duplica Tener un padre o un hermano diagnosticado es uno de los indicadores más sólidos en la evaluación de los factores de riesgo del cáncer de próstata. Si un familiar directo tuvo la enfermedad, tu probabilidad estadística se duplica. Si el diagnóstico del familiar ocurrió antes de los 55 años, el riesgo es aún mayor, ya que sugiere una variante genética con mayor penetrancia y precocidad. Mutaciones genéticas clave: Los genes BRCA1, BRCA2 y HOXB13 La ciencia ha identificado errores específicos en el mapa genético que actúan como potentes factores de riesgo para desarrollar cáncer prostático. Mutaciones BRCA: Aunque comúnmente se asocian al cáncer de mama, los hombres con mutaciones en los genes BRCA2 (y en menor medida BRCA1) tienen un riesgo significativamente elevado de desarrollar tumores prostáticos más agresivos. Gen HOXB13: Esta mutación está ligada específicamente al cáncer de próstata de inicio temprano. Detectar estas alteraciones permite a los especialistas diseñar una estrategia de vigilancia personalizada mucho antes de que aparezcan los primeros signos clínicos. Cáncer de próstata hereditario vs. casos esporádicos Es importante diferenciar entre el cáncer «esporádico» (que aparece por factores ambientales o edad) y el «hereditario». El cáncer hereditario representa aproximadamente entre el 5% y el 10% de los casos. Estos pacientes suelen presentar una evolución distinta, lo que nos obliga a considerar herramientas diagnósticas de mayor sensibilidad, como la biopsia por fusión, para asegurar una detección en etapas curativas. ¿La alimentación y el sobrepeso aumentan el riesgo? Factores de estilo de vida y metabolismo. A diferencia de la genética, los elementos metabólicos son componentes donde el paciente tiene capacidad de intervención. Sin embargo, la ciencia es clara: el entorno químico que creamos en nuestro cuerpo a través de los hábitos diarios puede consolidarse como uno de los factores de riesgo del cáncer de próstata más influyentes en la progresión de la enfermedad. Obesidad abdominal: Un motor de inflamación crónica
Diferencias entre cáncer de próstata e hiperplasia benigna: ¿Cómo distinguirlos?
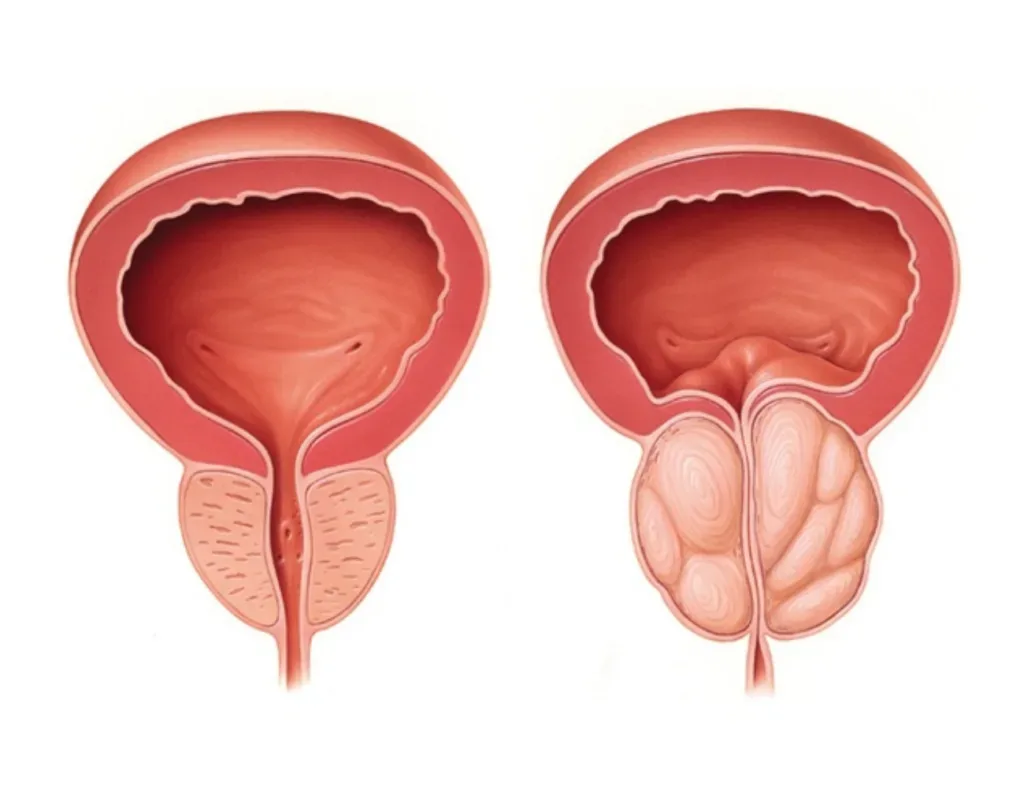
Diferencias entre cáncer de próstata e hiperplasia benigna: ¿Cómo distinguirlos? Para la mayoría de los hombres mayores de 50 años, notar cambios en su forma de orinar es una experiencia común. Sin embargo, surge de inmediato una pregunta que genera gran inquietud: ¿estos síntomas indican un crecimiento normal por la edad o son señales de algo más grave? Establecer las diferencias entre cáncer de próstata e hiperplasia benigna es el primer paso para recuperar la tranquilidad. Aunque ambas condiciones afectan a la misma glándula y pueden compartir algunas manifestaciones clínicas, sus causas, comportamientos biológicos y tratamientos son radicalmente distintos. Entender estas distinciones no solo ayuda a reducir la ansiedad, sino que permite al paciente tomar decisiones informadas sobre su salud urológica. ¿Qué es la hiperplasia benigna y en qué se diferencia del cáncer de próstata? Para comprender las diferencias entre cáncer de próstata e hiperplasia, lo primero que debemos entender es que la próstata no es un tejido estático. Con el paso de los años, la glándula experimenta cambios celulares, pero no todos esos cambios representan un riesgo para la vida. Crecimiento celular benigno vs. proliferación maligna La Hiperplasia Benigna de Próstata (HBP) es, como su nombre lo indica, un crecimiento no canceroso. Se trata de un aumento en el número de células normales que, al acumularse, expanden el tamaño de la glándula. Es un proceso tan común que se considera parte natural del envejecimiento masculino. Por el contrario, el cáncer de próstata implica una proliferación maligna. Aquí, las células sufren mutaciones genéticas que las hacen dividirse sin control y les otorgan la capacidad de invadir tejidos cercanos o incluso viajar a otros órganos (metástasis). Mientras que la hiperplasia solo «crece», el cáncer tiene el potencial de «invadir». Ubicación del problema: La zona de transición vs. la zona periférica Una de las mayores diferencias entre cáncer de próstata e hiperplasia radica en el lugar exacto donde se originan dentro de la glándula: Zona de Transición (HBP): La hiperplasia ocurre generalmente en la parte central de la próstata, la zona que rodea la uretra (el conducto por donde sale la orina). Al crecer hacia adentro, comprime la uretra rápidamente, lo que explica por qué la HBP suele dar síntomas urinarios muy pronto. Zona Periférica (Cáncer): La mayoría de los tumores malignos se originan en la periferia, es decir, en la parte externa de la próstata. Al estar lejos de la uretra, el cáncer puede crecer durante años sin obstruir el paso de la orina, lo que lo convierte en una enfermedad silenciosa que solo se detecta mediante estudios preventivos. Síntomas comunes: ¿Es posible distinguir el cáncer de próstata de la hiperplasia? Aunque ambas condiciones afectan la micción, la forma en que se presentan los síntomas es una de las principales diferencias entre cáncer de próstata e hiperplasia. Mientras que la hiperplasia es «ruidosa» y molesta, el cáncer suele ser un enemigo silencioso en sus etapas más tratables. Obstrucción urinaria y flujo débil: La señal clásica de la HBP Como mencionamos, la hiperplasia comprime la uretra desde el centro. Esto genera síntomas obstructivos que el paciente nota de inmediato: Goteo terminal: Dificultad para terminar de orinar. Nicturia: Necesidad de levantarse varias veces por la noche. Pujo vesical: Necesidad de hacer esfuerzo para iniciar el chorro. Sensación de vaciado incompleto: Sentir que «se quedó algo» después de ir al baño. Estos síntomas son molestos pero, en la gran mayoría de los casos, apuntan a un crecimiento benigno y no a una malignidad. El silencio del cáncer de próstata en etapas iniciales Aquí es donde radica la importancia de los estudios preventivos. Debido a que el tumor maligno suele crecer en la periferia de la glándula, no suele comprimir la uretra hasta que ya es muy grande o está avanzado. Por ello, es común que un paciente con un tumor agresivo no presente ningún síntoma urinario. Las diferencias entre cáncer de próstata e hiperplasia nos enseñan que «sentirse bien» no es garantía de estar sano en la salud prostática. ¿Desea profundizar en este tema? Si gusta revisar más sobre las señales de alerta y cómo se manifiesta esta patología, le invitamos a consultar nuestro artículo especializado: Sintomas del cáncer de próstata Señales de alerta roja: Hematuria y dolor óseo Cuando el cáncer comienza a dar síntomas, estos suelen ser distintos a los de la hiperplasia y requieren atención inmediata: Hematuria o hemospermia: Presencia de sangre en la orina o en el semen. Dolor óseo: Especialmente en la espalda baja o cadera, lo cual podría indicar que la enfermedad ha salido de la próstata. Disfunción eréctil de inicio súbito: Si no hay otra causa aparente, debe ser evaluada por un especialista. Diagnóstico diferencial: ¿Cómo saber si es cáncer o crecimiento benigno? Debido a que los síntomas pueden solaparse, los especialistas utilizamos un protocolo de diagnóstico diferencial para establecer con precisión las diferencias entre cáncer de próstata e hiperplasia. No se trata de una sola prueba, sino de un análisis integral de la salud de la glándula. El papel del PSA (Antígeno Prostático Específico) en ambas condiciones El PSA es una proteína producida por la próstata. Es un error común pensar que un PSA elevado significa cáncer automáticamente. En la hiperplasia, el PSA puede elevarse simplemente porque hay «más próstata» (más células produciendo la proteína). En el cáncer de próstata, el PSA se eleva porque las células malignas «fugan» más proteína al torrente sanguíneo. Para notar la diferencia, los especialistas analizamos la densidad del PSA (relación entre el nivel de antígeno y el tamaño de la glándula) y su velocidad de ascenso en el tiempo. Tacto rectal y Ultrasonido: Evaluando la textura y el volumen A través del tacto rectal, el urólogo puede percibir la consistencia de la glándula: Una próstata con hiperplasia suele sentirse blanda, lisa y elástica, aunque aumentada de tamaño. Una próstata con cáncer puede presentar zonas endurecidas, nódulos o una pérdida de la simetría. El ultrasonido, por su parte, nos ayuda a medir el volumen exacto para confirmar si la elevación
Biopsia por fusión para el diagnóstico del cáncer de próstata: Precisión milimétrica
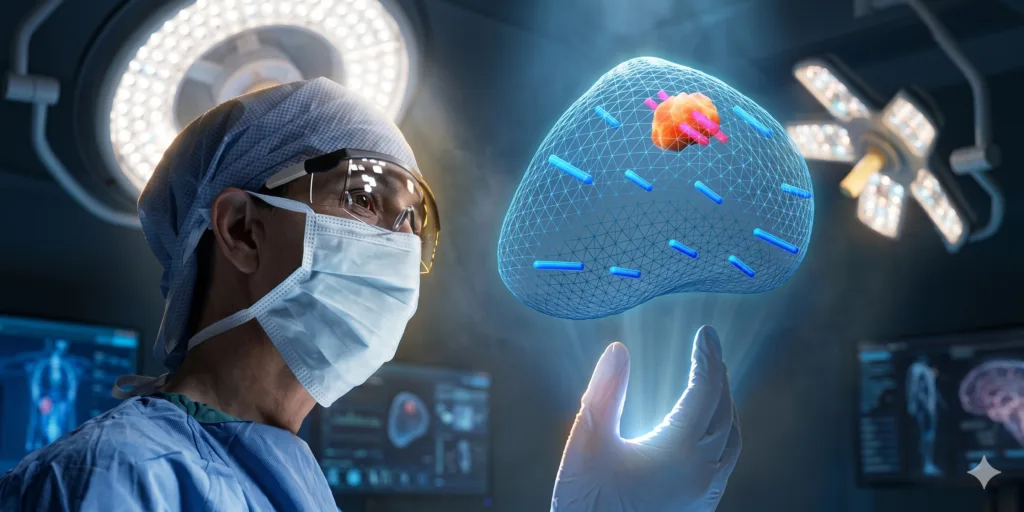
Biopsia por fusión para el diagnóstico del cáncer de próstata: Precisión milimétrica Durante décadas, la biopsia de próstata convencional se realizó de forma aleatoria, tomando muestras de diferentes zonas de la glándula con la esperanza de encontrar células malignas. Sin embargo, este método «a ciegas» presentaba un margen de error considerable. Hoy, la biopsia por fusión para el diagnóstico del cáncer de próstata representa el avance más importante en urología diagnóstica. Al combinar la potencia de la imagen digital con la precisión quirúrgica, esta tecnología permite localizar tumores que antes eran invisibles, ofreciendo al paciente una certeza diagnóstica sin precedentes y eliminando la necesidad de procedimientos repetitivos e innecesarios. ¿Qué es la biopsia por fusión y cómo revoluciona el diagnóstico? La biopsia por fusión no es un examen común; es un procedimiento de alta ingeniería médica que fusiona dos estudios distintos en uno solo para crear un mapa tridimensional de la próstata. La unión de la Resonancia Magnética y el Ultrasonido El secreto de esta tecnología radica en la «fusión» de imágenes: Resonancia Magnética Multiparamétrica (rmM): Antes del procedimiento, se obtiene una imagen de alta resolución que identifica zonas sospechosas con una precisión que el ultrasonido simple no alcanza. Ultrasonido en Tiempo Real: Durante la biopsia, el médico utiliza el ultrasonido para guiar la aguja. El Software de Fusión: Un sistema computarizado superpone la imagen de la resonancia sobre el ultrasonido en vivo. Esto permite que el urólogo vea exactamente dónde está la lesión sospechosa y dirija la muestra hacia ese punto específico. ¿Por qué es superior a la biopsia convencional (TRUS)? En una biopsia tradicional, se toman muestras siguiendo un patrón estándar, lo que puede pasar por alto tumores pequeños o ubicados en zonas difíciles. La biopsia por fusión para el diagnóstico del cáncer de próstata aumenta la tasa de detección de cánceres clínicamente significativos en más de un 30% en comparación con los métodos antiguos. En lugar de «pescar» en toda la glándula, el especialista va directamente al blanco, reduciendo el trauma al tejido sano y proporcionando resultados mucho más confiables. ¿Cómo se realiza el procedimiento de biopsia por fusión de próstata? Entender los pasos de la biopsia por fusión ayuda al paciente a sentirse más tranquilo y a comprender por qué este método es tan preciso. A diferencia de un examen rápido, este procedimiento es una intervención planificada digitalmente. Mapeo mediante Resonancia Magnética Multiparamétrica Todo comienza días antes de la intervención. El paciente se somete a una Resonancia Magnética de alta resolución. En este estudio, el radiólogo marca las zonas sospechosas (denominadas PI-RADS), creando un «mapa de calor» del tumor. Sin este mapa previo, la biopsia por fusión para el diagnóstico del cáncer de próstata no sería posible, ya que es el plano que guiará al médico. El software de fusión y la toma de muestras dirigida Ya en la sala de intervención, bajo sedación para que el paciente no sienta ninguna molestia, ocurre la magia tecnológica: El software carga la Resonancia Magnética previa. El urólogo realiza un ultrasonido en vivo. El sistema «fusiona» ambas imágenes, permitiendo que el médico vea la lesión sospechosa (que antes era invisible en el ultrasonido) como un objetivo claro en la pantalla. Se toman muestras milimétricas exactamente del centro y la periferia de la lesión. Preparación y cuidados posteriores para el paciente Al ser un procedimiento mínimamente invasivo, la recuperación es rápida. Generalmente, se requiere: Ayuno y una limpieza intestinal previa. Profilaxis antibiótica para evitar cualquier riesgo de infección. Reposo relativo de 24 a 48 horas tras el procedimiento. Es normal observar un ligero rastro de sangre en orina o semen durante unos días, pero la precisión de la técnica reduce significativamente las complicaciones en comparación con las biopsias repetitivas del pasado. ¿Para qué pacientes está recomendada la biopsia por fusión? No todos los pacientes necesitan una biopsia por fusión de inicio, pero se ha convertido en el estándar de oro para casos específicos donde la duda clínica persiste. Elevación persistente del PSA sin diagnóstico claro: Si un paciente tiene el Antígeno Prostático alto, pero las biopsias convencionales anteriores salieron negativas, la biopsia por fusión para el diagnóstico del cáncer de próstata es indispensable para encontrar tumores ocultos en zonas anteriores de la glándula. Pacientes en protocolos de Vigilancia Activa: Aquellos hombres que ya tienen un diagnóstico de cáncer de muy bajo riesgo y han decidido no operarse, necesitan esta tecnología para asegurarse de que el tumor no ha cambiado su agresividad biológica. Re-biopsia ante sospecha clínica: Cuando el médico «siente» algo irregular en el tacto rectal o el PSA sigue subiendo, la precisión de la fusión evita el ciclo de «biopsias repetidas» que solo causan estrés y cicatrización en la próstata. Ventajas clave: ¿Por qué elegir la tecnología de fusión? Optar por una biopsia por fusión para el diagnóstico del cáncer de próstata no es solo elegir un estudio moderno, es elegir la mayor probabilidad de éxito desde el primer paso. Las ventajas frente al método tradicional son determinantes para el futuro del paciente. Reducción de diagnósticos falsos negativos El mayor temor de un paciente con el PSA elevado es que le digan «no tienes nada» y que, meses después, el tumor aparezca en una etapa avanzada. La biopsia convencional suele pasar por alto hasta un 30% de los tumores agresivos. La tecnología de fusión reduce drásticamente este margen de error al asegurar que la muestra provenga del tejido realmente sospechoso, eliminando la incertidumbre de los falsos negativos. Menor número de punciones y mayor seguridad En una biopsia tradicional, al no saber dónde está el tumor, se suelen tomar muchas muestras «al azar» para intentar cubrir toda la glándula. Con la biopsia por fusión, al tener un objetivo identificado por la resonancia, se requieren menos punciones para obtener un diagnóstico certero. Esto se traduce en: Menor inflamación de la glándula. Reducción del riesgo de infecciones post-procedimiento. Una recuperación mucho más cómoda para el paciente. Clasificación exacta del Grado de Gleason Para decidir el tratamiento (cirugía, radioterapia o vigilancia), es
Sintomas del cáncer de próstata

Síntomas del cáncer de próstata: señales de alerta, evolución y diagnóstico clínico oportuno. Cuando se habla de los síntomas del cáncer de próstata es fundamental entender una característica clave de esta enfermedad: en la mayoría de los casos, su desarrollo es silencioso. A diferencia de otros padecimientos que generan dolor inmediato o alteraciones evidentes, el cáncer prostático puede avanzar lentamente durante años sin provocar molestias claras. Este comportamiento biológico es precisamente lo que hace que muchos hombres retrasen la evaluación médica. Existe la idea de que “si no duele, no es grave”. Sin embargo, en urología sabemos que la ausencia de dolor no significa ausencia de enfermedad. Conocer los síntomas del cáncer de próstata no tiene como objetivo generar alarma, sino darte herramientas para reconocer cambios importantes y tomar decisiones informadas sobre tu salud. ¿Cómo comienzan los síntomas del cáncer de próstata? El cáncer de próstata se origina cuando ciertas células de la glándula comienzan a multiplicarse de manera descontrolada. En etapas tempranas, estas alteraciones son microscópicas y no afectan de forma significativa la función urinaria ni el bienestar general. Durante esta fase inicial, el tumor puede estar completamente localizado y no generar ningún síntoma perceptible. De hecho, muchos diagnósticos tempranos se realizan a través de estudios de rutina, como el antígeno prostático específico (PSA), antes de que aparezca cualquier manifestación clínica. A medida que el tejido tumoral aumenta de tamaño, puede modificar la estructura interna de la próstata. Si el crecimiento ocurre en zonas cercanas a la uretra, comienzan a presentarse cambios urinarios. Si la enfermedad progresa más allá de la cápsula prostática, pueden aparecer síntomas adicionales. Entender esta evolución progresiva ayuda a comprender por qué la detección oportuna es tan importante. Síntomas urinarios del cáncer prostático: qué cambios debes observar. Entre los síntomas de cáncer de próstata más frecuentes se encuentran las alteraciones en el patrón urinario. Estas no suelen aparecer de manera abrupta; más bien se desarrollan lentamente, lo que puede hacer que el paciente las normalice con el tiempo. Alteraciones en el flujo y frecuencia miccional El paciente puede notar que el chorro urinario pierde fuerza o que tarda más tiempo en iniciar la micción (vacilación). En ocasiones, se requiere un mayor esfuerzo abdominal para lograr vaciar la vejiga por completo. Es común experimentar la sensación de vaciamiento incompleto, un aumento en la frecuencia urinaria o la necesidad de levantarse varias veces durante la noche (nicturia). Estos síntomas no son exclusivos del cáncer; también están presentes en la hiperplasia prostática benigna (HPB). Por ello, el contexto clínico y los estudios complementarios son determinantes para un diagnóstico preciso. Sangre en la orina o en el semen: una señal de alerta urológica La aparición de sangre en la orina (hematuria) o en el semen (hemospermia) siempre debe ser motivo de valoración médica inmediata. Aunque no siempre está relacionada con una neoplasia, constituye una señal de alarma que requiere un protocolo diagnóstico estructurado. En el contexto del cáncer de próstata, estas manifestaciones pueden aparecer cuando existe una alteración en la vascularización prostática o invasión de estructuras cercanas. Sin embargo, también pueden deberse a infecciones, inflamación o procedimientos recientes. El punto clave es no ignorar este hallazgo, ya que indica una alteración en el tracto urinario que debe ser investigada. Antígeno prostático elevado y su relación con los síntomas del cáncer de próstata. Cuando se sospecha una alteración prostática, el estudio más solicitado es el Antígeno Prostático Específico (PSA). Esta proteína es producida por la próstata y puede elevarse cuando existe mayor actividad celular. Es importante aclarar que un PSA elevado no confirma por sí solo un diagnóstico de cáncer. Puede aumentar en casos de inflamación, infección o crecimiento benigno de la glándula. Por ello, la interpretación del PSA debe hacerse dentro de un contexto clínico completo. La evaluación médica puede incluir repetición del análisis, cálculo del porcentaje de PSA libre, tacto rectal y estudios de imagen. El PSA es una herramienta de alerta, no un veredicto definitivo. Diagnóstico del cáncer de próstata: más allá de los síntomas. Cuando existen síntomas persistentes, PSA elevado o hallazgos sospechosos en la exploración física, se inicia un proceso estructurado de biopsia por fusión para el diagnóstico del cáncer de próstata. Actualmente, el abordaje diagnóstico moderno puede incluir: Resonancia magnética multiparamétrica, que permite identificar lesiones sospechosas dentro de la glándula. Clasificación mediante sistema PI-RADS para evaluar el nivel de riesgo. Biopsia prostática dirigida en caso de hallazgos relevantes. Este enfoque permite detectar lesiones clínicamente significativas con mayor precisión que en el pasado y reduce la probabilidad de diagnósticos innecesarios. El objetivo no es solo confirmar la presencia de células malignas, sino determinar su agresividad y comportamiento biológico para planear el tratamiento más adecuado. ¿Cómo diferenciar cáncer de próstata de hiperplasia benigna? Una de las dudas más frecuentes en pacientes con síntomas urinarios es saber si lo que presentan corresponde a cáncer o a crecimiento benigno de la próstata. Ambas condiciones pueden compartir síntomas como flujo urinario débil, dificultad para iniciar la micción o aumento en la frecuencia urinaria. Sin embargo, su comportamiento biológico es distinto. La hiperplasia prostática benigna suele generar un crecimiento uniforme de la glándula que comprime la uretra, pero no invade tejidos ni produce metástasis. En cambio, el cáncer puede desarrollarse de manera focal, formando áreas endurecidas que solo pueden detectarse mediante estudios especializados. Si quieres profundizar en este punto, puedes consultar nuestro artículo sobre [diferencias entre cáncer de próstata e hiperplasia benigna], donde se explican los criterios clínicos y diagnósticos que permiten distinguir ambas entidades. La conclusión es clara: los síntomas por sí solos no permiten establecer el diagnóstico definitivo. Síntomas en etapas avanzadas del cáncer prostático. Cuando el cáncer no se detecta en fases tempranas y progresa fuera de la próstata, pueden aparecer síntomas sistémicos. Entre los sintomas del cancer de prostata más relevantes se encuentran el dolor óseo —especialmente en columna lumbar o pelvis—, pérdida de peso involuntaria, fatiga persistente y debilidad en extremidades inferiores. Estos síntomas suelen estar relacionados con diseminación metastásica, particularmente hacia hueso, que
Biopsia de próstata por fusión de imágenes

Biopsia de próstata por fusión de imágenes. La biopsia de próstata por fusión de imágenes representa uno de los mayores avances en el diagnóstico moderno del cáncer de próstata. Gracias a la integración de tecnologías de imagen de alta resolución, este procedimiento permite identificar lesiones sospechosas con mayor exactitud, reduciendo diagnósticos erróneos y mejorando la toma de decisiones clínicas. A diferencia de las biopsias tradicionales, este método combina resonancia magnética multiparamétrica y ultrasonido en tiempo real, logrando un enfoque dirigido, preciso y personalizado. Como resultado, se incrementa la detección de cáncer clínicamente significativo y se evita la realización de procedimientos innecesarios. En este artículo conocerás en qué consiste la biopsia, cuándo se indica, cómo funciona la fusión de imágenes, qué tecnología se utiliza y por qué se ha convertido en el estándar más avanzado para el diagnóstico del cáncer de próstata. ¿Qué es una biopsia y para qué sirve? Una biopsia es un procedimiento médico que consiste en la extracción de una pequeña muestra de tejido de un órgano específico. Posteriormente, dicha muestra se analiza en un laboratorio de anatomía patológica para identificar alteraciones celulares, procesos inflamatorios o la presencia de cáncer. En el caso de la próstata, la biopsia es la única forma definitiva de confirmar o descartar cáncer de próstata. Aunque existen estudios de laboratorio y métodos de imagen que sugieren sospecha, el diagnóstico final depende del análisis histopatológico del tejido. Limitaciones de la biopsia de próstata tradicional Biopsia guiada por ultrasonido transrectal (TRUS) Durante muchos años, la biopsia tradicional guiada por ultrasonido transrectal fue el método estándar. Este procedimiento se basa en la toma sistemática de múltiples muestras de la próstata sin identificar con claridad las lesiones sospechosas. Sin embargo, este enfoque presenta importantes limitaciones: No visualiza con precisión los tumores Puede pasar por alto lesiones clínicamente significativas Genera falsos negativos Aumenta el número de punciones innecesarias Puede detectar cánceres indolentes sin relevancia clínica Por estas razones, surgió la necesidad de un método más preciso y dirigido. ¿Qué es la biopsia de próstata por fusión de imágenes? La biopsia de próstata por fusión de imágenes es un procedimiento avanzado que integra las imágenes obtenidas por resonancia magnética con el ultrasonido en tiempo real. Esta fusión permite dirigir las punciones exactamente a las lesiones sospechosas, aumentando la precisión diagnóstica. A diferencia de la biopsia tradicional, este método no toma muestras al azar, sino que se enfoca en áreas previamente identificadas como de alto riesgo. ¿Cómo funciona la fusión de imágenes? El procedimiento consta de varios pasos clave: Adquisición de imágenes por resonancia magnética multiparamétrica Identificación y marcaje de lesiones sospechosas Carga de las imágenes al sistema de fusión Integración con ultrasonido en tiempo real Navegación precisa dentro de la próstata Obtención dirigida de muestras de tejido Este proceso garantiza que las biopsias se realicen exactamente en las zonas de mayor sospecha clínica. Ventajas de la biopsia de próstata por fusión de imágenes Entre los principales beneficios de este procedimiento destacan: Mayor detección de cáncer de próstata clínicamente significativo Menor número de punciones Reducción de falsos negativos Menor riesgo de complicaciones Diagnósticos más certeros Mejor planificación terapéutica Estas ventajas hacen que la biopsia de próstata por fusión de imágenes sea considerada actualmente como el estándar de oro en el diagnóstico prostático avanzado. Sistema Artemis: innovación y precisión Una de las plataformas más reconocidas a nivel mundial para la biopsia de próstata por fusión de imágenes es el sistema Artemis. Este sistema destaca por ser semi-robótico y por su alta precisión en la navegación prostática. En México, es una de las tecnologías más avanzadas disponibles para la realización de este tipo de biopsias ¿Cómo funciona el sistema Artemis? El sistema Artemis integra múltiples plataformas de imagen para ofrecer un procedimiento seguro y altamente preciso. Entre sus principales características se encuentran: Fusión exacta de imágenes de resonancia magnética y ultrasonido Registro tridimensional de la próstata Navegación ecográfica avanzada Control preciso de cada punción Además, el sistema almacena la longitud y ubicación exacta de cada muestra, lo que permite conocer el tamaño y evolución de las lesiones a lo largo del tiempo. ¿Quién debería considerar una biopsia de próstata por fusión de imágenes? Este procedimiento está especialmente indicado en: Pacientes con un nivel de antígeno prostático (PSA) elevado y creciente, pero con una o más biopsias tradicionales negativas. La información detallada proporcionada por la fusión de la imagen de resonancia magnética (MRI) con la del ultrasonido (US) puede llevar al médico al área más sospechosa de la enfermedad, lo que aumenta las posibilidades de obtener una biopsia exitosa. Pacientes que han experimentado una biopsia tradicional o cognitiva una o más veces y desean mejorar la sensibilidad y especificidad del diagnóstico de cáncer, si persiste la sospecha. Pacientes que buscan identificar el tamaño, la ubicación y el alcance exactos del cáncer de próstata. Pacientes que buscan ayudar a confirmar la etapa y el grado de su cáncer de próstata. Pacientes que eligen controlar un bajo grado de cáncer de próstata para retrasar el tratamiento (vigilancia activa). Se puede planificar la terapia focal de un paciente (radioterapia, crioablación, electroporación irreversible), ya que es importante que el tratamiento se concentre en el área afectada. Una biopsia por fusión de imágenes de MRI y US puede proporcionar una imagen en 3D clara para ayudar al oncólogo y/o urólogo a guiar la terapia más adecuada para un paciente en particular. Pacientes que tienen una recurrencia local, indicada por un nivel alto de PSA, después de una prostatectomía radical, radiación, crioablación, electroporación irreversible (Nanoknife) o ablación con láser. La biopsia por fusión de imágenes puede evaluar toda el área en busca de tejido anormal. La indicación final debe ser evaluada por un urólogo especializado. Biopsia de próstata en México La biopsia de próstata por fusión de imágenes ha transformado el diagnóstico del cáncer de próstata. Gracias a la integración de resonancia magnética y ultrasonido, este procedimiento ofrece mayor precisión, seguridad y confiabilidad, permitiendo detectar tumores relevantes y mejorar el pronóstico del
Tratamientos para el cáncer de próstata

Tratamientos para el Cáncer de Próstata Antes de conocer los tratamientos para el Cáncer de Próstata, conozcamos la próstata. La próstata es una glándula del tamaño de una nuez ubicada entre la vejiga y el pene. La próstata está justo enfrente del recto. La uretra, atraviesa el centro de la próstata, desde la vejiga hasta el pene, dejando que la orina fluya fuera del cuerpo. La próstata, secreta un líquido que nutre y protege los espermatozoides. Durante la eyaculación, la próstata aprieta este líquido en la uretra y es expulsado con los espermatozoides como semen. Los conductos deferentes llevan los espermatozoides desde los testículos a las vesículas seminales. Las vesículas seminales aportan líquido al semen durante la eyaculación. Estudios y exámenes de la Próstata Examen rectal digital (DRE): un médico inserta un dedo en el recto y palpa la próstata. A veces, un DRE puede detectar agrandamiento de la próstata, bultos o nódulos de cáncer de próstata, o sensibilidad por prostatitis. Antígeno prostático específico (PSA): la próstata produce una proteína llamada PSA, que se puede medir mediante un análisis de sangre. Si el PSA es alto, es más probable que haya cáncer de próstata, pero un agrandamiento de la próstata también puede causar un PSA alto. Ultrasonido de próstata (ecografía transrectal): se inserta una sonda de ecografía en el recto, acercándolo a la próstata. A menudo, la ecografía se realiza con una biopsia para detectar el cáncer de próstata. Biopsia de próstata: se inserta una aguja en la próstata para extraer tejido y detectar cáncer de próstata. Por lo general, esto se hace a través del recto. Biopsia de próstata por fusión. La Biopsia de próstata por fusión de imágenes se basa en el sistema Artemis. El único sistema semirobótico que existe en México para la realización de este tipo de biopsias. Es un sistema útil en la detección, planificación de tratamientos focales y en el seguimiento de pacientes con cáncer de próstata en vigilancia activa. Consiste en la integración a través de diferentes plataformas, de las imágenes obtenidas con resonancia magnética (RM) y ultrasonido, para mejorar la seguridad de la biopsia de próstata dirigiendo las punciones a las lesiones observadas. Por lo tanto, el sistema Artemis determina y almacena la longitud de cada punción, con lo que se puede conocer el tamaño del tumor detectado para las futuras biopsias durante el seguimiento de los pacientes. Artemis permite registrar y guardar los sitios de las biopsias permitiendo volver a biopsiar la misma lesión en un futuro, por ejemplo, en los casos en que se está realizando seguimiento activo de un cáncer diagnosticado previamente. Enfermedades más comunes de la Próstata Prostatitis: inflamación de la próstata, a veces causada por una infección. Por lo general, se trata con antibióticos. Próstata agrandada: llamado hipertrofia prostática benigna o HPB, el crecimiento de la próstata afecta prácticamente a todos los hombres mayores de 50 años. Los síntomas, como dificultad para orinar, tienden a aumentar con la edad. Los medicamentos o la cirugía pueden tratar la HPB. Cáncer de próstata: es la forma más común de cáncer en los hombres, pero solo uno de cada 41 hombres muere de cáncer de próstata. Se pueden usar cirugía, radiación, terapia hormonal y quimioterapia para tratar el cáncer de próstata. Algunos hombres optan por retrasar el tratamiento, lo que se denomina espera vigilante. Tratamientos para el cáncer de próstata Crioablación La crioablación, es un tratamiento mínimamente invasivo que usa un frío intenso para congelar y destruir un tejido enfermo, incluyendo las células cancerosas. Durante la crioterapia, se hace fluir gas de argón a alta presión dentro de un aplicador (una criosonda), creando un frío intenso (se crea una «bola de hielo») que se pone en contacto con el tejido enfermo.La crioterapia puede aplicarse tópicamente (sobre la superficie de la piel), en forma percutánea (a través de la piel) o quirúrgicamente. En algunos casos se requiere una incisión quirúrgica. Puesto que la crioterapia consiste en una serie de pasos que conducen a la muerte celular, los tumores se congelan y se descongelan repetidamente; típicamente se usan dos o más ciclos de congelar y descongelar. Una vez que las células tumorales se han destruido, los glóbulos blancos del sistema inmune trabajan para eliminar el tejido muerto.Este procedimiento es una opción de tratamiento eficaz para los pacientes que podrían tener dificultades durante la cirugía. Todo el procedimiento es muy rápido y normalmente se completa dentro de una a tres horas. Electroporación Irreversible En la actualidad, el único sistema de electroporación irreversible comercializado a nivel mundial se denomina NanoKnife®. La técnica se lleva a cabo bajo anestesia general y bloqueo muscular, y puede realizarse mediante cirugía abierta, laparoscópica o por vía percutánea. La técnica consiste en colocar electrodos en la zona a tratar, con una distancia entre los mismos de 1,5 o 2 cm para crear un campo eléctrico necesario para el tratamiento. Cada ciclo consiste en pulsos cortos (90 mS) de un alto voltaje de corriente continua (90 Amp) y se espera un tiempo entre la aplicación de distintos ciclos (un ciclo suele completarse en menos de 2 minutos). La potencia total entre cada par de electrodos oscila entre los 1500 y los 3000 Voltios. Algunas contraindicaciones de la electroporación irreversible son arritmias cardiacas, pacientes portadores de algún tipo de dispositivo implantable, evitándose las ablaciones próximas a dichos dispositivos. La electroporación es una opción de tratamiento eficaz para los pacientes que podrían tener dificultades durante la cirugía. El procedimiento de electroporación suele tener una duración aproximada de 2-3 horas, incluyendo el tiempo de preparación y de visualización de la zona de ablación por medio de técnicas de imagen. ¿Cuándo acudir con el médico? Concierte una cita con su médico si tiene algún signo o síntoma que le preocupe. Continúa el debate sobre los riesgos y beneficios de la detección del cáncer de próstata, y las organizaciones médicas difieren en sus recomendaciones. Hable con su médico sobre la detección del cáncer de próstata. Juntos, pueden decidir qué es lo mejor para usted.
Para que sirve la próstata

¿Para que sirve la próstata? ¿Para que sirve la próstata? La próstata es una glándula del tamaño de una nuez ubicada entre la vejiga y el pene. La próstata está justo enfrente del recto. La uretra, atraviesa el centro de la próstata, desde la vejiga hasta el pene, dejando que la orina fluya fuera del cuerpo. La próstata, secreta un líquido que nutre y protege los espermatozoides. Durante la eyaculación, la próstata aprieta este líquido en la uretra y es expulsado con los espermatozoides como semen. Los conductos deferentes llevan los espermatozoides desde los testículos a las vesículas seminales. Las vesículas seminales aportan líquido al semen durante la eyaculación. Análisis de la próstata Examen rectal digital (DRE): un médico inserta un dedo en el recto y palpa la próstata. A veces, un DRE puede detectar agrandamiento de la próstata, bultos o nódulos de cáncer de próstata, o sensibilidad por prostatitis. Antígeno prostático específico (PSA): la próstata produce una proteína llamada PSA, que se puede medir mediante un análisis de sangre. Si el PSA es alto, es más probable que haya cáncer de próstata, pero un agrandamiento de la próstata también puede causar un PSA alto. Ultrasonido de próstata (ecografía transrectal): se inserta una sonda de ecografía en el recto, acercándolo a la próstata. A menudo, la ecografía se realiza con una biopsia para detectar el cáncer de próstata. Biopsia de próstata: se inserta una aguja en la próstata para extraer tejido y detectar cáncer de próstata. Por lo general, esto se hace a través del recto. Enfermedades más comunes Una vez entendiendo para que sirve la próstata, podemos identificar las enfermedades más comunes: Prostatitis: inflamación de la próstata, a veces causada por una infección. Por lo general, se trata con antibióticos. Próstata agrandada: llamado hipertrofia prostática benigna o HPB, el crecimiento de la próstata afecta prácticamente a todos los hombres mayores de 50 años. Los síntomas, como dificultad para orinar, tienden a aumentar con la edad. Los medicamentos o la cirugía pueden tratar la HPB. Cáncer de próstata: es la forma más común de cáncer en los hombres, pero solo uno de cada 41 hombres muere de cáncer de próstata. Se pueden usar cirugía, radiación, terapia hormonal y quimioterapia para tratar el cáncer de próstata. Algunos hombres optan por retrasar el tratamiento, lo que se denomina espera vigilante. ¿Qué es el Cáncer de Próstata? El cáncer de próstata es un cáncer que se produce en la próstata, una pequeña glándula con forma de nuez, que produce el líquido seminal que nutre y transporta los espermatozoides.El cáncer de próstata, es uno de los tipos de cáncer más comunes en los hombres. Por lo general, el cáncer de próstata crece lentamente e inicialmente se limita a la glándula prostática, donde es posible que no cause daños graves. Sin embargo, mientras que algunos tipos de cáncer de próstata crecen lentamente y pueden necesitar un tratamiento mínimo o incluso ningún tratamiento, otros tipos son agresivos y pueden diseminarse rápidamente. Síntomas del Cáncer de Próstata Los síntomas del cáncer de próstata pueden incluir: Necesidad de orinar con más frecuencia, a menudo durante la noche. Necesidad de correr al baño. Dificultad para empezar a orinar (vacilación) Esforzarse o tomarse mucho tiempo al orinar. Flujo débil. Sensación de que la vejiga no se ha vaciado por completo. Sangre en la orina o sangre en el semen. ¿Qué causa el cáncer? No se sabe exactamente qué causa el cáncer de próstata, aunque varias situaciones pueden aumentar su riesgo de desarrollar la afección.Éstos incluyen: Edad: el riesgo aumenta a medida que envejece y la mayoría de los casos se diagnostican en hombres mayores de 50 años.Grupo étnico: el cáncer de próstata es más común entre los hombres de ascendencia africana y caribeña que entre los hombres asiáticosAntecedentes familiares: tener un hermano o un padre que desarrolló cáncer de próstata antes de los 60 años parece aumentar su riesgo de desarrollarlo.Obesidad: investigaciones recientes sugieren que puede haber un vínculo entre la obesidad y el cáncer de próstata. Una dieta equilibrada y el ejercicio regular pueden reducir el riesgo de desarrollar cáncer de próstata.Dieta: se están realizando investigaciones sobre los vínculos entre la dieta y el cáncer de próstata, y existe alguna evidencia de que una dieta rica en calcio está relacionada con un mayor riesgo de desarrollar cáncer de próstata. Tratamiento para el cáncer focalizado La ablación tiene como objetivo mantener el beneficio oncológico de las opciones de tratamiento activo y reducir el riesgo de efectos secundarios mediante la preservación del tejido no canceroso. La situación anatómica de la próstata la convierte en un órgano accesible por diferentes vías (transuretral, transperineal, transrectal, suprapúbica), por lo que siempre ha constituido un órgano atractivo para aplicar, lo que genéricamente podemos denominar, tratamientos ablativos mínimamente invasivos. Una vez que sabemos para que sirve la próstata, sus caracteristicas y tipo de cáncer es importante considerar las nuevas maneras de tratamiento. La ablación con frio (crioablación prostática), demuestra algunos beneficios con respecto a otros tratamientos empleados en el cáncer de próstata: respeta las estructuras vecinas, la pérdida de sangre es mínima y representa una alternativa en aquellos pacientes no idóneos para cirugía o radioterapia. Además, existe la posibilidad del tratamiento del cáncer de próstata, con la ablación con impulsos eléctricos (Electroporación Irreversible), la cual ha demostrado seguridad y viabilidad de esta técnica, con bajos efectos secundarios del paciente, libre de metástatisis y 100% de sobrevida. La electroporación irreversible realiza una ablación del tejido tumoral mediante la administración de una corriente directa de alto voltaje entre un par de electrodos. Al dirigirse al tumor, con múltiples pulsos eléctricos consecutivos, la membrana de las células de cáncer se vuelve irreversiblemente permeable, lo que resulta en la muerte celular del tumor.